Effekt och kliniska data ONTOZRY® (cenobamat)1,2

ONTOZRY® (cenobamat) är indicerat som tilläggsbehandling av fokala anfall, med eller utan sekundär generalisering hos vuxna patienter med epilepsi, som inte kontrollerats tillräckligt trots tidigare behandling med minst två antiepileptiska läkemedel.1
ONTOZRY® har utvärderats i två randomiserade, dubbelblinda, placebokontrollerade multicenterstudier och i en öppen säkerhetsstudie med mer än 1900 patienter med kontrollerade fokala anfall.2-4
C017-studien2
Grundläggande information om C017-studien:
En dubbelblind, randomiserad, placebokontrollerad kompletterande multicenterstudie för att utvärdera effekt och säkerhet för Ontozry® hos patienter med behandlingsresistenta fokala anfall n = 437. Vuxna patienter (18–70) med fokala anfall trots behandling med 1–3 antiepileptika.
-
Baslinje
8 veckor
-
Titrering
Dubbelblind; 6 veckor
-
Underhåll
Dubbelblind; 12 veckor
-
Primära effektmått
- Responderfrekvens, definierat som en minskning av anfallsfrekvensen på 50 % eller mer under underhållsfasen
-
Sekundära effektmått
- 100% responderfrekvens
- Anfallsfrekvens efter anfallstyp
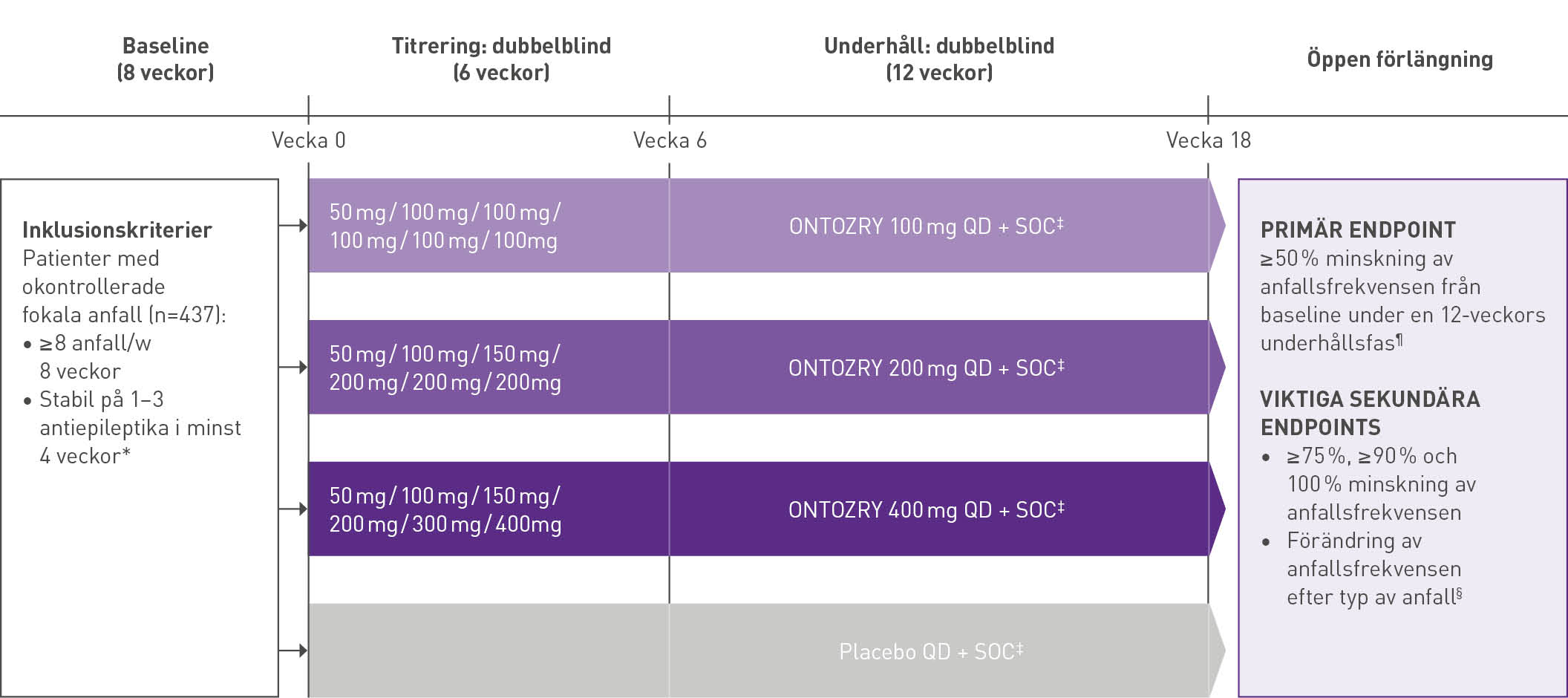
Primärt utfallsmått- ≥50% anfallsreduktion
En signifikant minskning av anfallsfrekvensen sågs hos 56,1% av patienterna som fick ONTOZRY® 200 mg + standardbehandling* jämfört med placebo + standardbehandling*, där motsvarande siffra var 25,5%.
Vid en dos på 400 mg ökade den 50-procentiga svarsfrekvensen till 64% jämfört med placebo på 25%.
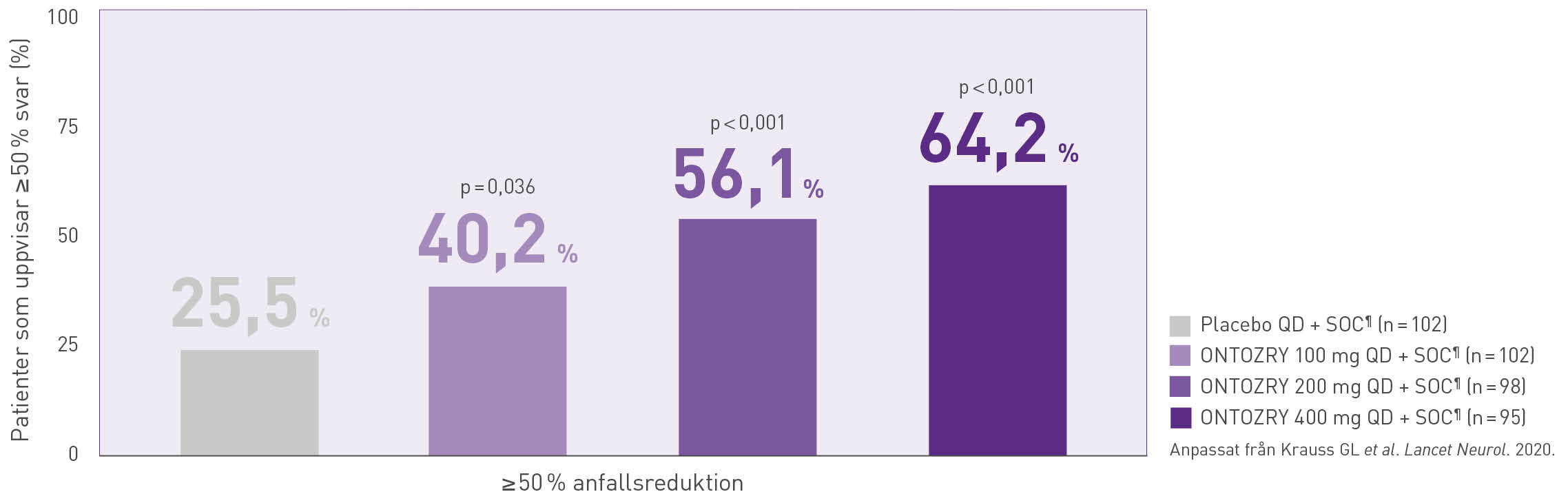
QD = en gång dagligen; SOC = standardbehandling * Standardbehandling var behandling med upp till 3 samtidiga antiepileptika.
Patienter kan bli anfallsfria med ONTOZRY1,2
28,6% av patienterna hade en minskning av anfallsfrekvensen ≥75% med 200 mg ONTOZRY® + standardbehandling* respektive en minskning med 45% med 400 mg + standardbehandling*.
17,3% respektive 28,4% uppnådde en ≥90% anfallsreduktion med 200 mg ONTOZRY® + standardbehandling* respektive 400 mg ONTOZRY® + standardbehandling*.
Anfallsfrihet påvisades hos 11,2% respektive 21,1% av patienterna som fick ONTOZRY® 200 mg respektive 400 mg + standardbehandling*, jämfört med 1% av dem som fick placebo + standardbehandling*.
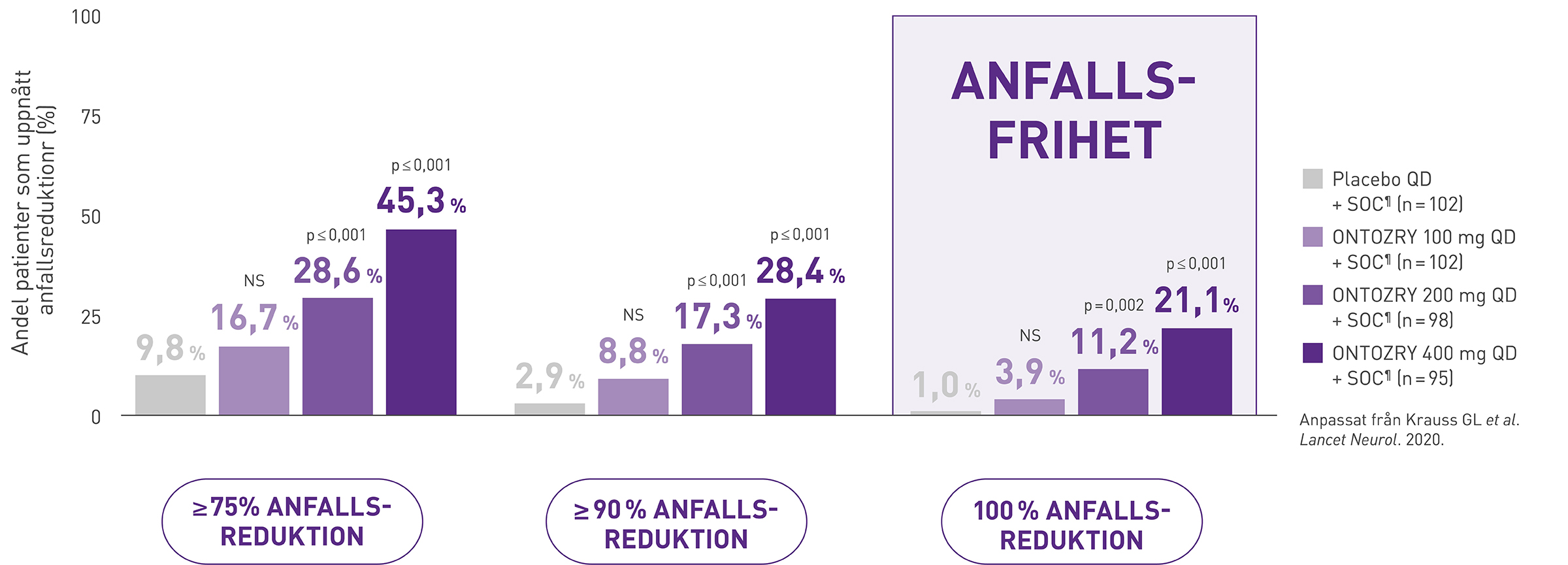
Liknande svar sågs i subgrupper som låg över eller under mediananfallsfrekvensen, samt i subgrupper med längre eller kortare sjukdomsduration än mediandurationen.
QD = en gång dagligen; SOC = standardbehandling
* Standardbehandling var behandling med upp till 3 samtidiga antiepileptika.

Cenobamate clinical overview
Dr. Elinor Ben-Menachem shares insights and experiences from clinical studies on cenobamate in this comprehensive lecture.
▼Detta läkemedel är föremål för utökad övervakning.
Ontozry® (cenobamat) 12,5 mg odragerad tablett samt 25 mg, 50 mg, 100 mg, 150 mg och 200 mg filmdragerade tabletter. Rx F. ATC-kod: N03AX25 - antiepileptika, övriga antiepileptika. Indikation: Ontozry är indicerat som tilläggsbehandling av fokala anfall, med eller utan sekundär generalisering hos vuxna patienter med epilepsi, som inte kontrollerats tillräckligt trots tidigare behandling med minst två antiepileptika. Kontraindikationer: Överkänslighet mot den aktiva substansen eller mot något hjälpämne, ärftligt kort QT-syndrom. Varningar: Patienter ska instrueras att uppsöka läkare om tecken på självmordstankar/självmordsbeteende uppstår, samt om tecken och symptom på läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) inträffar. Innehåller laktos. Cenobamat kan minska exponeringen av substanser som metaboliseras via CYP3A4, CYP2B6 samt öka exponeringen av substanser som metaboliseras via CYP2C19. Cenobamat rekommenderas inte till fertila kvinnor som inte använder preventivmedel eller vid amning. MAH: Angelini Pharma S.p.A. Lokal kontakt: Angelini Pharma Nordics, nordic.medinfo@angelinipharma.com. Datum för senaste översyn av SPC: 9/2025. För pris och ytterligare information, se www.fass.se.
- Produktresumé ONTOZRY
- Krauss GL et al. Lancet Neurol. 2020;19(1):38-48.
- Chung SS et al. Neurology. 2020;94(22):e2311-e2322.
- Sperling MR et al. Epilepsia. 2020;61(6):1099-108.
 HarmoniaMentis Sverige
HarmoniaMentis Sverige