Biverkningar och säkerhetsinformation ONTOZRY (cenobamat)

ONTOZRY® (cenobamat) är indicerat som tilläggsbehandling av fokala anfall, med eller utan sekundär generalisering hos vuxna patienter med epilepsi, som inte kontrollerats tillräckligt trots tidigare behandling med minst två antiepileptiska läkemedel.1
Biverkningar
ONTOZRY tolererades generellt väl med somnolens, yrsel, trötthet och huvudvärk som de vanligaste rapporterade biverkningarna.2
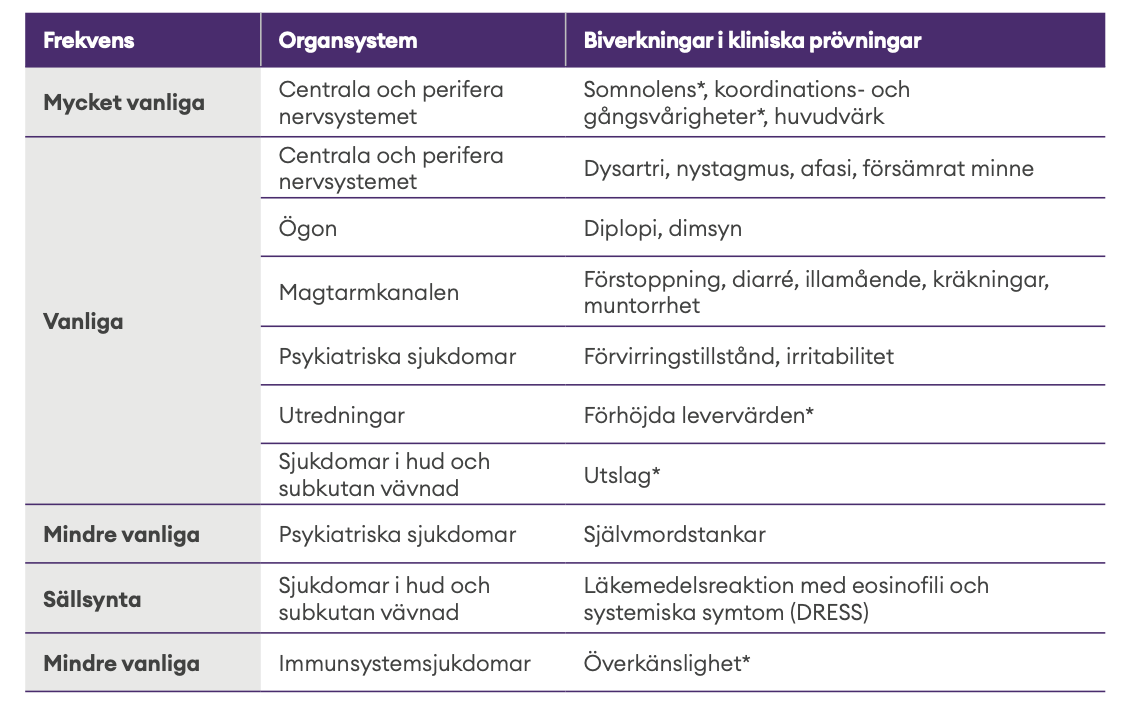
* Grupptermer:
Somnolens: Somnolens, trötthet, sedering och hypersomni; Koordinations- och gångsvårigheter: Yrsel, vertigo, balansrubbning, ataxi, gångstörning och onormal koordination; Överkänslighet: Överkänslighet, läkemedelsöverkänslighet, ögonlocksödem; Utslag: Utslag, erytematösa utslag, generaliserade utslag, makulära utslag, makulopapulösa utslag,
morbilliforma utslag, papulösa utslag, pruritiska utslag; Förhöjda levervärden: Förhöjt alaninaminotransferas, förhöjt aspartataminotransferas, förhöjda leverenzymer, onormal leverfunktion, förhöjda transaminaser
Förekomsten av biverkningar var dosrelaterad.2
Rapporterade biverkningar hos ≥5% som behandlades med ONTOZRY®1
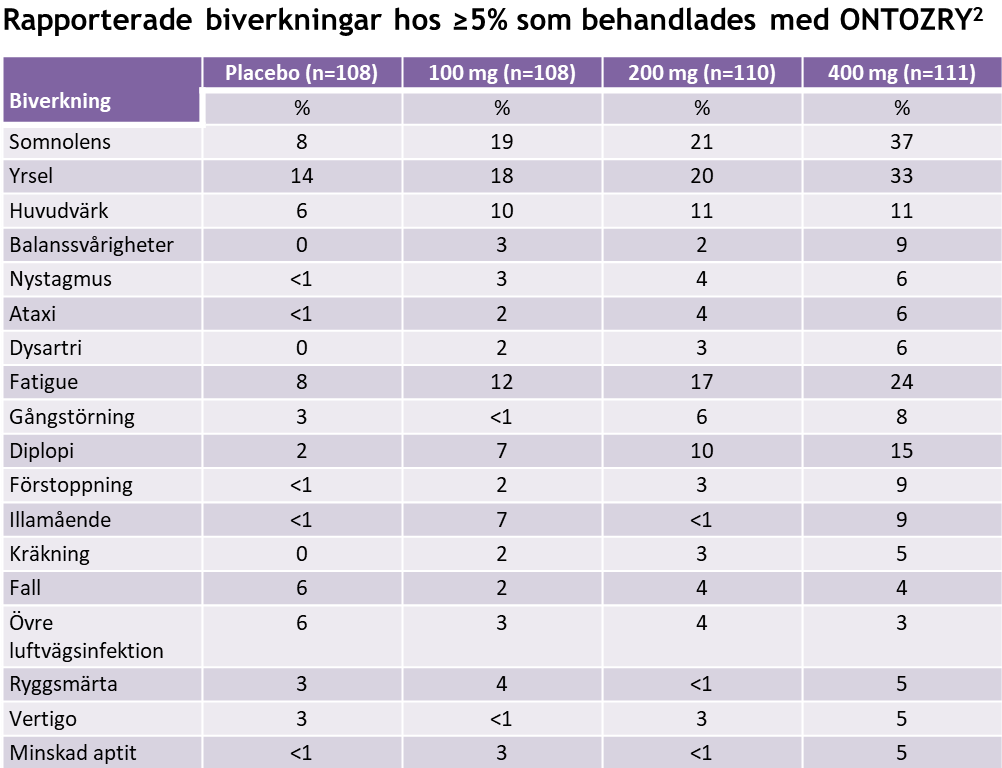
Anpassad från Krauss GL et al., Lancet Neurol. 2020
Varningar och försiktighet
DRESS2,3
Läkemedelsreaktion med eosinofili och systemiska symtom (DRESS), som kan vara livshotande eller dödlig, rapporterades i tre fall i samband med ONTOZRY® när det intitierades med högre doser (50 mg eller 100 mg dagligen) och titrerades snabbt (veckovis eller snabbare titrering). De tre fallen rapporterades inom två till fyra veckor efter påbörjad behandling. När ONTOZRY® initierades enligt rekommenderat doseringsschema med 12,5 mg/dag och titrerades varannan vecka, i en öppen säkerhetsstudie med 1 340 epilepsipatienter (studie C021), rapporterades inga fall av DRESS.2
Informera patienter som initieras på ONTOZRY® om tecken och symtom på DRESS och övervaka dem noggrant för hudreaktioner. Symtom på DRESS är bland annat feber, utslag associerade med påverkan på andra organsystem, lymfadenopati, onormala leverfunktionsprover och eosinofili. Om tecken och symtom som tyder på dessa reaktioner inträffar, ska ONTOZRY® omedelbart sättas ut och en alternativ behandling övervägas. ONTOZRY® ska alltid inledas med dosen 12,5 mg en gång dagligen och inte titreras oftare än en gång varannan vecka.
Förkortat QT-intervall2
Ärftligt kort QT-syndrom är ett sällsynt genetiskt syndrom, som förknippas med en ökad risk för plötslig död och kammararytmier, särskilt kammarflimmer. ONTOZRY® får inte användas till patienter med medfött kort QT-syndrom.
Vidare så har en dosberoende förkortning av QTcF-intervallet observerats med ONTOZRY® och läkare ska därför iaktta försiktighet vid förskrivning av ONTOZRY® i kombination av andra läkemedel som kan förkorta QT-intervallet.
Fertilitet, graviditet och amning2
Preventivmedel för män och kvinnor
ONTOZRY® rekommenderas inte till fertila kvinnor som inte använder preventivmedel. Fertila kvinnor som samtidigt använder p-piller ska använda ytterligare eller alternativa, icke-hormonella preventivmetoder under behandling med ONTOZRY® och fram till 4 veckor efter avslutad behandling.
Graviditet2
Risk förenad med epilepsi och antiepileptika i allmänhet:
Det har visat sig att hos barn till behandlade kvinnor med epilepsi, är prevalensen av missbildningar två till tre gånger högre än den andel på ca 3% som ses i den allmänna populationen. I den behandlade populationen har en ökning av missbildningar noterats med polyfarmaci. I vilken utsträckning behandlingen och/eller underliggande tillstånd har orsakat detta har dock inte klargjorts. Utsättning av behandling med antiepileptika kan leda till förvärrad sjukdom, vilket skulle kunna vara skadligt för modern och fostret.
Risk förenad med ONTOZRY®:
Det finns inte tillräckliga uppgifter från användning av ONTOZRY® hos gravida kvinnor.
ONTOZRY® skall användas under graviditet endast då tillståndet kräver att det är absolut nödvändigt att kvinnan behandlas med ONTOZRY®.
Amning2
Det är okänt om ONTOZRY® och dess metaboliter utsöndras i bröstmjölk.
Studier på råttor har visat att ONTOZRY® utsöndras i mjölken. En risk för det ammade barnet kan inte uteslutas. Som en försiktighetsåtgärd bör amning avbrytas under behandling med ONTOZRY®.
▼Detta läkemedel är föremål för utökad övervakning.
Ontozry® (cenobamat) 12,5 mg odragerad tablett samt 25 mg, 50 mg, 100 mg, 150 mg och 200 mg filmdragerade tabletter. Rx F. ATC-kod: N03AX25 - antiepileptika, övriga antiepileptika. Indikation: Ontozry är indicerat som tilläggsbehandling av fokala anfall, med eller utan sekundär generalisering hos vuxna patienter med epilepsi, som inte kontrollerats tillräckligt trots tidigare behandling med minst två antiepileptika. Kontraindikationer: Överkänslighet mot den aktiva substansen eller mot något hjälpämne, ärftligt kort QT-syndrom. Varningar: Patienter ska instrueras att uppsöka läkare om tecken på självmordstankar/självmordsbeteende uppstår, samt om tecken och symptom på läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) inträffar. Innehåller laktos. Cenobamat kan minska exponeringen av substanser som metaboliseras via CYP3A4, CYP2B6 samt öka exponeringen av substanser som metaboliseras via CYP2C19. Cenobamat rekommenderas inte till fertila kvinnor som inte använder preventivmedel eller vid amning. MAH: Angelini Pharma S.p.A. Lokal kontakt: Angelini Pharma Nordics, nordic.medinfo@angelinipharma.com. Datum för senaste översyn av SPC: 9/2025. För pris och ytterligare information, se www.fass.se.
- Krauss GL et al. Lancet Neurol. 2020;19(1):38-48.
- Produktresumé ONTOZRY®
- Sperling MR, et al. Epilepsia. 2021;62(12):3005-15
 HarmoniaMentis Sverige
HarmoniaMentis Sverige